Perché siamo così entusiasti dall’acido formico? Ne conosciamo realmente le potenzialità ed i rischi? Proviamo a fare un po’ di chiarezza e a dare alcune spiegazioni chimico-fisiche che possono aiutare nell’uso di tale principio attivo.
di Marco D’Imperio
Perché siamo così entusiasti dall’acido formico? Ne conosciamo realmente le potenzialità ed i rischi?
Proviamo a fare un po’ di chiarezza e a dare alcune spiegazioni chimico-fisiche che possono aiutare nell’uso di tale principio attivo.
Innanzitutto vanno ricordati quali sono i vantaggi derivanti dall’uso dell’acido formico:
- abbatte la varroa in fase foretica (probabilmente l’azione sulla varroa è data dall’effetto corrosivo dell’acido formico ed all’interruzione dei processi metabolici dopo inalazione da parte dell’acaro);
- contribuisce ad un buon abbattimento delle varroe sotto opercolo e può quindi essere utilizzato anche in presenza di covata (abbassa i tassi di accoppiamento/natalità della varroe; l’effetto non si manifesta solo con le cadute ma anche con le mancate nascite);
- nel momento di massima evaporazione, uccide le uova e le larve delle api ed arresta la deposizione della regina. In sostanza, induce quello che chiamiamo blocco di covata indotto con evidenti aumenti dell’efficacia;
- induce le api ad un maggiore comportamento igienico (a causa del blocco di covata indotto) e ciò ha come conseguenza un abbassamento delle cariche virali, fungine e batteriche;
- è un acido semplice ed in poco tempo degrada formando metaboliti innocui quali acqua e anidride carbonica;
- in piccolissime percentuali è già presente nel miele;
- è utilizzabile in apicoltura biologica.
Vi sono però anche degli svantaggi che non vanno sottovalutati:
- è un acido che causa scompensi alle api (anche se, va detto, non ci sono molti studi che valutano la farmacocinetica dell’acido sulle api);
- sebbene negli ambienti laboratoriali sia definito come un acido debole è, per gli usi comuni, una sostanza infiammabile e, ad alte concentrazioni, altamente corrosiva e dunque va maneggiato con cautela utilizzando gli opportuni dispositivi di protezione individuale (DPI);
- vi sono sospetti sulla sua cancerogenicità e sulla sua mutagenicità (studi che andrebbero approfonditi) e dunque i rischi per l’operatore vanno tenuti in seria considerazione.
Andiamo però ad analizzare più nel dettaglio alcuni aspetti/parametri che saranno utili ai fini di un uso consapevole dell’acido formico.
I DPI necessari per la manipolazione del formico
Come detto l’acido formico è una sostanza infiammabile e, ad alte concentrazioni, è anche altamente corrosivo.
Non di meno il rischio di rovinare indumenti e superfici è alto per cui anche a tal riguardo è opportuno prendere precauzioni.
Ma quali sono i DPI da adottare?
- maschera che copre bocca e naso con filtro per vapori organici ovvero quello con la classica striscia marrone (codice A –AX) che in genere è accoppiata alla striscia grigia (B), gialla (E) e verde (K) ed è utilizzabile anche per le sublimazioni con acido ossalico. Con la maschera facciale (respiratore) si risolve anche il problema degli occhiali. In caso di contatto dei vapori o dei liquidi con le vie respiratorie, procedere ad un abbondante risciacquo con acqua di rubinetto e alla successiva espulsione del liquido di risciacquo (non ingoiare). È importante dotarsi di dispositivi che rispettino le norme europee (EN 138÷149).
- In mancanza di una maschera che copre l’intero volto, è estremamente importante dotarsi di occhiali in plastica che coprono anche le parti laterali degli occhi. In caso di contatto del liquido con gli occhi, procedere ad un abbondante risciacquo con acqua di rubinetto.
- Guanti in nitrile anche riutilizzabili. Vanno bene anche quelli utilizzati per lavare i piatti a patto che siano
sufficientemente spessi. In caso di contatto del liquido con la pelle, procedere ad un abbondante risciacquo con acqua di rubinetto.

La temperatura di ebollizione
La temperatura di ebollizione dell’acido formico è 100,8 °C mentre quella dell’acqua distillata è di 100 °C. Va precisato che, per avere l’evaporazione di un solvente, non è necessario che si arrivi alla temperatura di ebollizione ovvero al punto in cui il fenomeno raggiunge il suo apice; l’evaporazione avviene anche a temperature più basse e in misura proporzionale alla temperatura.
Detto ciò, in una soluzione fatta da acido formico ed acqua avremo due componenti la cui temperatura di ebollizione, come detto, è molto simile a differenza di quanto avviene in altre miscele binarie (ad esempio toluene 110 °C e benzene 80 °C). La vicinanza delle due temperature di ebollizione fa sì che nei processi di evaporazione si formi quello che in gergo sia chiama azeotropo ovvero una miscela che, oltre un certo limite, non può essere più arricchita ovvero non si può arrivare, se non con particolari accorgimenti, alla completa separazione dei due componenti.
Ma perché ci interessa tanto la temperatura di ebollizione? Perché avere a che fare con una miscela azeotropica è per noi un vantaggio poiché ci garantisce che la concentrazione della soluzione di partenza che inseriamo nell’erogatore (es. 60%) rimarrà quasi inalterata durante il trattamento (10-15 gironi). Questo è ancor più vero se l’evaporazione avviene all’interno dell’arnia o ancor meglio del nido cioè a temperature più basse (35-45 °C) rispetto a quelle di ebollizione.
La densità
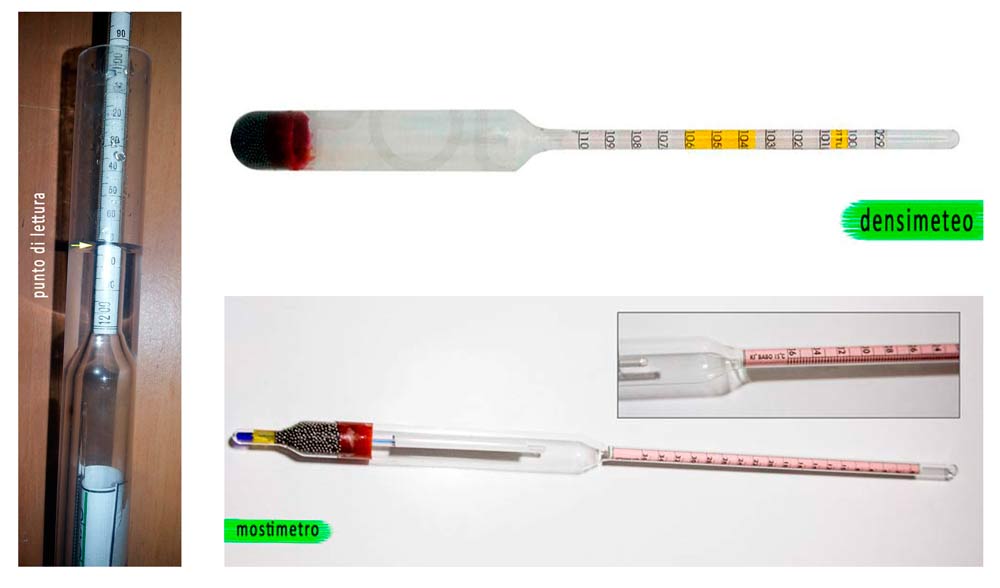
La densità dell’acido formico è pari a 1,22 g/cm3 ovvero 1220 g/L. Può essere misurata attraverso vari strumenti ed in commercio ne esistono di varia natura, da quelli professionali detti DENSIMETRI con ampie scale di misura a quelli più spartani tipo il MOSTIMETRO che si usa per misurare il grado alcolico/quantità di zuccheri nel mosto.
La misura si esegue nel seguente modo:
- riempire fino a metà il tubo all’interno del quale viene fornito lo strumento;
- inserire lo strumento avendo cura il tubo sia posto in posizione verticale rispetto all’orizzonte;
- aspettare qualche secondo che lo strumento in galleggiamento si stabilizzi;
- leggere la misura sull’apposita scala in corrispondenza del punto in cui lo strumento fuoriesce dal liquido.
In funzione della concentrazione e del tipo di strumento utilizzato possiamo avere le segu enti letture:
enti letture:
- soluzione al 100% di acido formico (nella pratica non realizzabile): sulla scala del densimetro si dovrebbe leggere il valore della densità pari a 1220; non è possibile misurare tale soluzione con i mostimetri perché il valore va fuori scala;
- soluzione all’85% di acido formico: sulla scala del densimetro si leggerà il valore della densità pari a 1187; non è possibile misurare tale soluzione con i mostimetri perché il valore va fuori scala;
- soluzione al 60% di acido formico: sulla scala del densimetro si leggerà il valore della densità pari a 1132; sulla scala mostimetro (in genere è quella rossa) si leggerà il valore pari a 27;
- soluzione al 50% di acido formico: sulla scala del densimetro si leggerà il valore della densità pari a 1110; sulla scala mostimetro (in genere è quella rossa) si leggerà il valore pari a 22,5.
Se volessimo controllare la rispondenza tra il valore nominale riportato in etichetta (es. 60%) e quello reale, dovremmo eseguire le misure, secondo le indicazioni riportate sui densimetri/mostimetri, alla temperatura di 20 °C.
Occorre a questo punto fare alcune considerazioni pratiche: non ha senso essere rigorosi in merito alla temperatura e cercare complicati fattori di correzione quando invece commettiamo altri errori, spesso di grossa entità, che vanificano di gran lunga la precisione che ricerchiamo con la temperatura. Per le nostre misure possono andare bene 20 ± 5 °C.
L’acqua
L’acqua che viene normalmente utilizzata in laboratorio per la diluizione delle soluzioni è distillata ovvero priva di sali minerali ed altre sostanze (non serve la purezza microbiologica). Ottima è l’acqua ottenuta dai deumidificatori dei quali si fa largo uso in apicoltura.
Tuttavia, anche in questo caso occorre mettere in campo il buon senso. Se venisse utilizzata l’acqua di rubinetto quali alterazioni si potrebbero avere? Innanzitutto verrebbero alterate le misure di densità le quali si basano sull’assunto che l’acqua distillata ha una densità pari ad 1 g/cm3 ovvero 1 kg/L. In secondo luogo verrebbe alterata la temperatura di ebollizione dell’acqua che non sarebbe più 100 °C ma sarebbe leggermente superiore (innalzamento ebullioscopico).
Altre interferenze potrebbero derivare dal fatto che l’acqua di rubinetto, contenendo una certa dose di sali minerali di varia natura (fra cui carbonati e bicarbonati), potrebbe dare origine a soluzioni tampone o a fenomeni di precipitazione che potrebbero alterare le concentrazioni del formico. Ciò nonostante sarebbero degli errori che potrebbero compensarsi e, soprattutto, anche ammettendo che la concentrazione del formico non sia proprio quella voluta ma leggermente differente, è facile supporre che l’efficacia contro al varroa non cambi in maniera sostanziale!
Le diluizioni
La diluizione di una soluzione più concentrata non è un’operazioni facile da eseguire. Tuttavia, con un po’ di
accortezza e con le adeguate cautele, è possibile giungere ad un risultato accettabile.
Innanzitutto occorre chiarire cosa si intende con 85%. È ovviamente una misura della concentrazione in cui il
formico è presente in una soluzione assieme all’acqua. Ma è cosa ben diversa dire che abbiamo a che fare con una soluzione all’85% in peso (p/p) o con una soluzione all’85% in volume (v/v). In commercio il formico viene venduto, nella stragrande maggioranza dei casi, al peso e dunque, se non esplicitamente riportato il contrario, quella concentrazione è da intendersi come 85% in peso ovvero 1 kg di soluzione contiene 850 g di formico e 150 g di acqua.
Per operare le opportune conversioni è utile sapere che:
- 1 kg di formico all’85% in p/p corrisponderà a 0,847 L di soluzione;
- 1 L di soluzione all’85% in p/p peserà 1,187 kg.
Dunque, per sapere quanti litri di soluzione all’85% in p/p si hanno a disposizione, basta pesare il liquido,
togliere la tara, e dividere il risultato per 1,187.
Come si possono eseguire le più comuni diluizioni partendo da 1 kg di soluzione all’85% in peso?
- se si aggiungono 400 mL= 400 g di acqua distillata si otterrà una soluzione al 61% in peso;
- se si aggiungono 417 mL= 417 g di acqua distillata si otterrà una soluzione al 60% in peso;
- se si aggiungono 500 mL= 500 g di acqua distillata si otterrà una soluzione al 57% in peso;
- se si aggiungono 600 mL= 600 g di acqua distillata si otterrà una soluzione al 53% in peso;
- se si aggiungono 700 mL= 700 g di acqua distillata si otterrà una soluzione al 50% in peso;
Nel calcolo sopra indicato si è assunto di utilizzare acqua distillata la cui densità è di 1 kg/L (a 20 °C).
Tuttavia, come già detto in precedenza, anche utilizzando acqua di rubinetto la cui densità è leggermente superiore (1,015 kg/L di media), l’errore che si commette può essere considerato trascurabile per gli scopi apistici.
Inoltre, si è partiti dall’assunto che la concentrazione dell’acido formico di partenza sia esattamente l’85% in peso ma difficilmente tale valore è preciso (molto spesso è inferiore ed in alcuni caso può essere più bassa anche di alcuni punti percentuale). Sarebbe dunque opportuno verificare la densità con il densimetro o con il mostimetro della soluzione di partenza e/o quella della soluzione finale.
È bene ribadire che, nonostante in quest’articolo vengano forniti tutti gli elementi per operare a “regola d’arte”, per gli scopi di abbattimento della varroa (che non sono scopi analitici) non è necessario raggiungere un livello elevato di precisione della concentrazione.
L’umidità relativa e la temperatura nei processi di evaporazione
I parametri che regolano i processi di evaporazione sono l’umidità relativa e la temperatura. I due parametri sono strettamente collegati e non ha senso parlare solo di umidità (U% o RH%) o solo di temperatura. Del resto, la definizione di umidità relativa (percentuale di vapore che l’aria possiede rispetto a quella massima che potrebbe contenere a saturazione, ad una determinata temperatura) lascia intuire tale intimo legame. Dunque, quando si dice che l’aria ha un’umidità del 20%, si dovrebbe specificare a quale temperatura.
Detto questo, perché tali parametri sono importanti nell’evaporazione del formico. Perché avere umidità relative troppo basse con temperature elevate può portare ad evaporazioni troppo violente con due conseguenze: 1) il “margine di lavoro” per il processo di evaporazione è molto ampio ed in tali casi si può verificare un rapido esaurimento del liquido all’interno degli erogatori; 2) la famiglia reagisce formando la barba fuori dall’arnia e, nei casi peggiori, si ha la morte della regina e/o delle api.
Al contrario avere umidità relative troppo elevate può significare: 1) che il “margine di lavoro” del processo di
evaporazione è piccolo e dunque l’evaporazione potrebbe richiedere troppo tempo; 2) che siamo vicini alle condizioni di saturazione (100% di umidità relativa) e ciò porterebbe alla condensazione della soluzione e quindi allo sviluppo di una “pioggia acida” che potrebbe non far piacere ad api e regina (rischio di orfanità o, nei casi peggiori, morte della famiglia). Tuttavia possiamo affermare, in base alle esperienze degli ultimi anni, che quest’ultima condizione si verifica raramente all’interno dell’arnia, a patto che la famiglia sia forte e dunque sia in grado di ventilare adeguatamente.
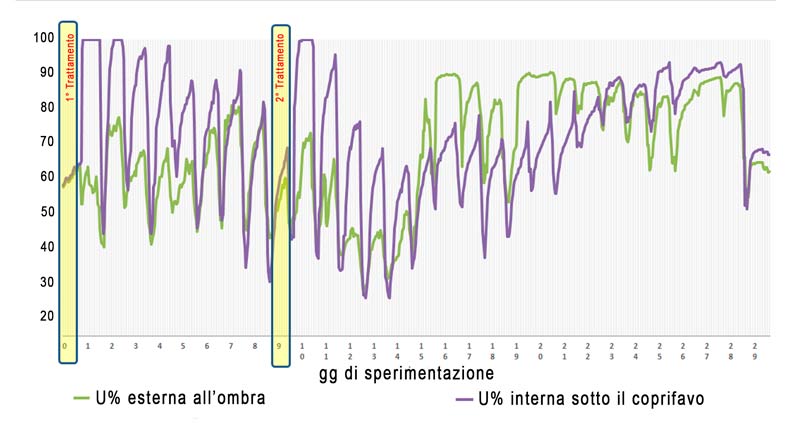
In tutto questo occorre considerare che le condizioni di umidità relativa e temperatura cambiano nel corso della giornata come mostrato nel diagramma dell’umidità 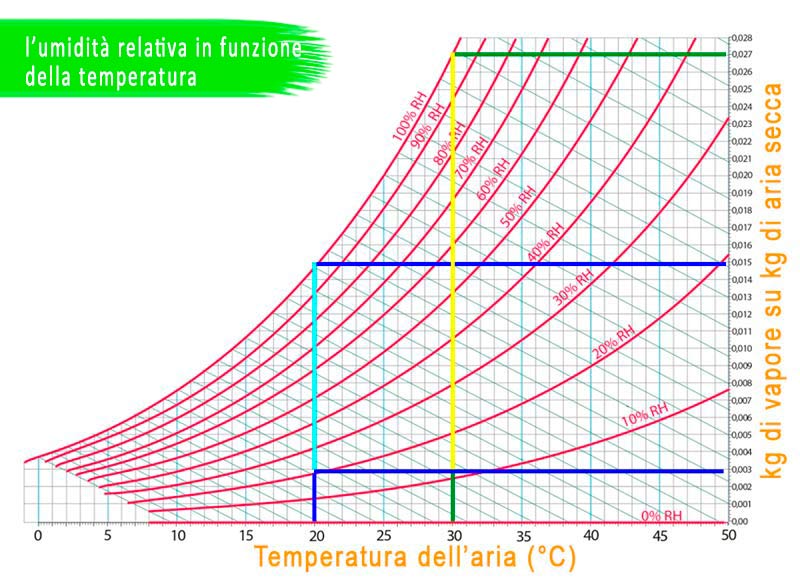 relativa: ad esempio, alle 7.00 di mattina, un’aria a 20°C che ha il 20% di umidità relativa (3 g di vapore su kg di aria secca) può accettare circa 12 g di vapore per kg di aria secca prima di arrivare a saturazione; alle 12.00, la temperatura aumenta fino ad arrivare, ad esempio, a 30 °C. In queste condizioni, quella stessa aria della mattina non ha più il 20% di umidità relativa ma quasi del 10% e soprattutto può accettare ben 24 g di vapore per kg di aria secca prima di arrivare a saturazione con conseguente accelerazione dei processi di evaporazione.
relativa: ad esempio, alle 7.00 di mattina, un’aria a 20°C che ha il 20% di umidità relativa (3 g di vapore su kg di aria secca) può accettare circa 12 g di vapore per kg di aria secca prima di arrivare a saturazione; alle 12.00, la temperatura aumenta fino ad arrivare, ad esempio, a 30 °C. In queste condizioni, quella stessa aria della mattina non ha più il 20% di umidità relativa ma quasi del 10% e soprattutto può accettare ben 24 g di vapore per kg di aria secca prima di arrivare a saturazione con conseguente accelerazione dei processi di evaporazione.
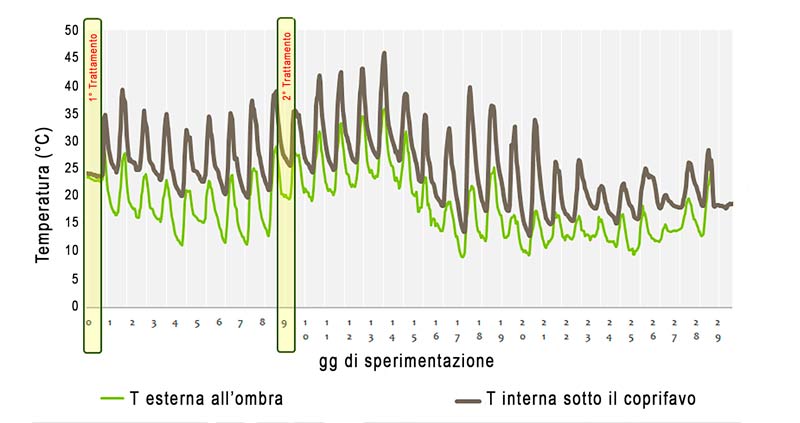
Quindi come regolarsi con le temperature e l’umidità? Innanzitutto è bene evitare temperature troppo elevate (superiori a 25-28 °C misurate all’esterno e all’ombra) e/o giornate troppo secche perché fanno consumare velocemente il principio attivo e rendono meno efficace il trattamento oltre che più rischioso per le api. Va tenuto presente che le temperature interne all’arnia, misurate sopra il nido/sotto il coprifavo, possono essere anche di 10 gradi superiori a quelle esterne misurate all’ombra.
L’esperienza degli ultimi anni ci ha insegnato ad avere meno paura delle condizioni opposte ovvero basse temperature ed elevate umidità (condizioni che si possono verificare in corrispondenza di giornate piovose o con nebbia). Tali giornate rallentano i processi di evaporazione e dunque, come accorgimento, potrebbe essere necessario allungare il periodo del trattamento. È comunque sconsigliabile eseguire l’intero trattamento in tali condizioni perché si potrebbe avere una riduzione dell’efficacia.
Metodi di somministrazione
I metodi di somministrazione dell’acido formico sono numerosi e spesso bizzarri. In rete si trovano numerosi
erogatori e/o metodi più o meno artigianali.
Se tuttavia si possono accettare delle piccole deroghe sulle concentrazioni, forse conviene essere più rigidi
sugli erogatori ed affidare le sorti di un apiario a strumenti testati ed affidabili ovvero ad erogatori che consentono un rilascio lento e costante del principio attivo.
Fra quelli maggiormente utilizzati dagli addetti ai lavori, citiamo:
- l’erogatore tedesco Nassenheider il quale è autoregolante: con alte temperature l’evaporazione avviene unicamente sul cartoncino verticale e quindi su una bassa superficie; con le basse temperature il liquido fa in tempo a migrare lungo il cartoncino e a gocciolare nella vaschetta dove c’è il panno; in quest’ultimo caso la superficie evaporante aumenta e va a compensare le minori quantità di acido formico evaporate a causa delle temperature inferiori; ha l’inconveniente di essere composto da numerosi piccoli pezzi e di richiedere una cornice supplementare (melario) da inserire sul nido che, unitamente al coprifavo capovolto, consente il suo posizionamento.
- L’erogatore cosiddetto “novarese” o Aspronovar il quale sposta il processo di evaporazione all’interno del nido dove le api posso termoregolare la temperatura e quindi stabilizzare l’umidità; ciò, almeno in linea di principio, potrebbe portare ad un’evaporazione più uniforme e graduale; in questo caso si può modulare l’evaporazione del principio attivo aumentato o diminuendo l’altezza dello stoppino che fuoriesce della bottiglietta.
- L’erogatore alla pugliese o cosiddetto dei “poveri” (cit. Savino Petruzzelli) il quale è molto simile a quello novarese con la differenza che le bottigliette che contengono il formico sono più basse e schiacciate (ciò potrebbe richiedere, per il suo posizionamento, uno spazio maggiore di quello di un singolo favo); anche in questo caso si può modulare l’evaporazione del principio attivo aumentato o diminuendo l’altezza dello stoppino che fuoriesce della bottiglietta.


